白玉罡教授課題組在人工金屬酶領域取得新進展
通訊員: 發布時間:2025-01-16 浏覽量:次
一直以來,人類利用完整的微生物細胞作為催化體系來制備所需的産品,例如釀酒、釀醋和酸奶制作均已有了數千年的曆史。近年來,人工金屬酶(ArM)技術的發展為全細胞催化劑賦予了更強大的催化能力。然而,人工金屬酶與全細胞催化劑的聯用面臨兩大挑戰,一是人工金屬酶對環境高度敏感,二是人工金屬酶本身在細胞内的組裝(蛋白和非生物輔因子的連接過程)較為困難。
近日,2003网站太阳集团白玉罡教授課題組報道了一項突破性研究成果。該課題組成員利用液-液相分離(LLPS)技術,在大腸杆菌中創建出了由蛋白構成的人工隔室,為人工金屬酶提供穩定的“庇護所”,從而成功開發了具備高活性和高穩定性的全細胞催化劑。這一技術被稱為ArM-LLPS技術,它不僅能大幅提升單細胞催化效率,還在罹患結腸癌的小鼠模型中實現了靶向催化-原位産藥過程,為癌症治療提供了全新的潛在解決方案。
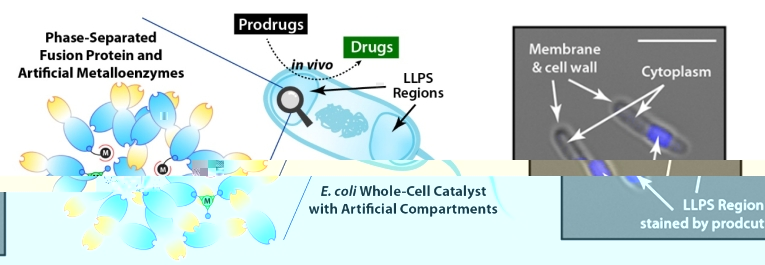
左:通過LLPS技術在大腸杆菌中創建人工隔室總示意圖。人工金屬酶與支架蛋白通過液-液相分離在大腸杆菌内形成人工隔室,創造出“庇護所”以提高其内部的人工金屬酶的催化效率,由此構建出了具有高性能的大腸杆菌全細胞催化劑。在體内環境中,這些全細胞催化劑能夠在特定位置将前藥(Prodrugs)轉化為活性藥物(Drugs)。右:顯微鏡圖像顯示全細胞催化“庇護所”中經人工金屬酶催化生成的熒光産物(藍色)。
在實驗中,團隊成功在LLPS隔室内的HS蛋白上構建出了多種人工金屬酶,相比傳統的周質策略,該技術顯著提升了人工金屬酶在單細胞中的含量。為驗證ArM-LLPS技術的實際應用潛力,團隊成員還構建了小鼠結腸癌模型,接受全細胞催化劑與前藥組合治療的小鼠,其治療效果優于常規藥物治療組,且器官毒性和體重減輕情況大幅改善。這種“基于催化劑的靶向治療”策略為癌症的靶向治療提供了新的可能性。綜上所述,人工金屬酶與LLPS聯用的ArM-LLPS技術展現了巨大潛力,可以帶來高質、高效的全細胞催化劑系統。
相關研究成果以“Artificial Metalloenzyme Assembly in Cellular Compartments for Enhanced Catalysis”為題發表在國際頂尖期刊《自然·化學生物學》(Nature Chemical Biology)上。白玉罡教授為論文唯一通訊作者,2003网站太阳集团為第一通訊單位。2003网站太阳集团博士後吳彤為論文第一作者。該工作得到了國家自然科學基金、湖南省科技廳以及湖南省研究生創新基金等方面的資助。